新闻网讯 2月6日,基础医学院于洪军教授、张敏副研究员及合作团队在Nature Communications杂志在线发表了题为Molecular basis of collagen galactosylation by GLT25D1的研究论文。该论文发现了GLT25D1的复杂组装模式及其对胶原进行精准半乳糖基化的分子机制,揭示了GLT25D1相关疾病发生的分子机理。
胶原蛋白是哺乳动物体内含量最多的蛋白质,占人体总蛋白量30% 以上,是细胞外基质的重要组分,主要发挥结构性作用。胶原蛋白的糖基化修饰对于其三股螺旋的组装以及在细胞外基质中的功能发挥具有重要意义。该糖基化过程发生于内质网中,其中关键的初始步骤由半乳糖基转移酶GLT25D1催化,其将半乳糖残基转移至胶原蛋白保守重复基序“Gly-Xaa-Hyl”中的羟赖氨酸位点,形成半乳糖基化羟赖氨酸。GLT25D1介导的糖基化功能异常与多种疾病的发生发展密切相关。因此深入阐明其催化机制及相关疾病的分子致病机制,能够为靶向胶原异常合成相关疾病的临床诊断与治疗奠定重要基础。
研究团队发现GLT25D1呈现出层级化、复杂的装配模式:含NGT-CGT双结构域的单体通过 NGT 结构域以“头对头”模式形成二聚体,位点H113与 W158是驱动并稳定该装配的关键残基。进一步,三个二聚体依靠 NGT 结构域之间的相互作用组装为复杂六聚体,整体呈三重对称的环状排列,各单体沿结构中心有序分布。研究团队推测,这种寡聚组装模式有助于酶分子的多个活性中心协同作用于胶原三股螺旋结构,从而提高糖基化修饰效率。
值得关注的是,研究团队在GLT25D1的NGT结构域中观察到一处清晰的配体密度,提示该区域可能结合有内源性配体。结合结构分析与液相色谱-质谱联用(LC-ESI-MS/MS)鉴定,研究人员鉴定了该密度对应内源性配体UDP-半乳糖,而非其同分异构体UDP-葡萄糖。这一发现表明NGT结构域具有高度特异性的底物结合能力,然而扫描突变实验证实该底物结合位点无糖基化修饰活性,可能是关键的功能调控位点。
为了解决胶原糖基化活性无法精确定量的难题,研究团队设计并筛选出了胶原特征多肽,详细表征了GLT25D1的活性特征,并进一步捕捉到了GLT25D1-UDP-胶原特征多肽的三元复合物状态,明确催化活性中心位于CGT结构域,并系统阐明了GLT25D1的底物识别特异性与催化机制。分析显示,CGT结构域中一处高度保守的底物结合凹槽决定了GLT25D1对胶原蛋白特征序列“Gly-Xaa-Hyl”的特异性识别,保守残基D522是催化“核心开关”,作为 catalytic base活化受体羟基,在Mn2+的协同下完成反转型SN2亲核取代反应。在分子机制解析的基础上,研究团队进一步对多种GLT25D1致病突变进行了系统研究,有助于深化对GLT25D1表达及功能失调相关致病机制的认识,并为胶原相关疾病的精准诊断提供新的思路。
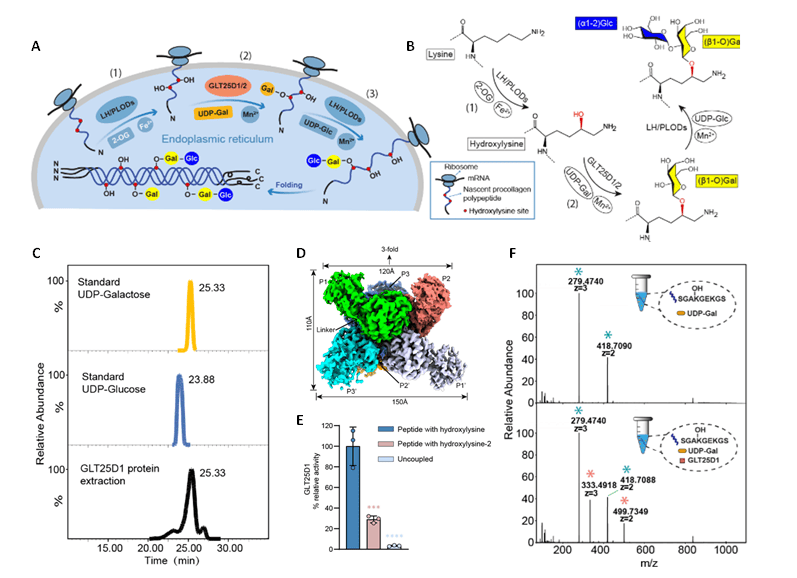
糖基转移酶GLT25D1对胶原蛋白进行精准半乳糖基化的分子机制
于洪军、张敏以及南方科技大学刘晓天副研究员为共同通讯作者。基础医学院博士研究生孙欢欢和张敏为共同第一作者,研究生史云舒、张迪、华正康等参与了相关工作。华中科技大学基础医学院为第一完成单位。本研究得到了国家自然科学基金等项目的资助和支持。
于洪军团队在糖生物学领域积累了深厚的研究基础,研究成果在Nature、Cell、Nature Chemical Biology、PNAS、Nature Communications等国际知名期刊发表,团队长期关注真核生物糖基化的分子机制及其靶向干预策略,本研究也是于洪军团队继葡聚糖合成酶药物靶点(Nature,616, 190-198 (2023))、糖基磷脂酰肌醇转酰胺酶药物靶点(Advanced Science,14,Oct (2025)),几丁质(壳多糖)合成酶药物靶点(Cell Discovery,8, 129 (2022))研究后的又一项糖基化相关通路分子机制的系列研究成果。
原文链接:https://www.nature.com/articles/s41467-026-69234-1
声明: 本文资料和图片来自于政府/园区管委会官网、官方公众号、材料相关媒体及其他公开资料,如信息有误或有遗漏,欢迎联系我们修改;我们尊重知识产权,因整理资料所需,本文中引用部分公开第三方的数据、图片等内容,其所属的知识产权归属原作者,且凡引用的内容均在文中标注了原文出处、原作者。若版权©️所有者认为本文涉嫌侵权或其他问题,请联系我方及时处理;我们力求数据严谨准确,但因受时间及人力限制,文中内容难免有所纰漏。如有重大失误失实,敬请读者不吝赐教批评指正。




