- 英文名称:Laminin (925-933);Laminin-derived peptide CDPGYIGSR;Laminin α1 chain fragment (925-933)
- 中文名称:层粘连蛋白 (925-933) 片段;层粘连蛋白 α1 链九肽片段(CDPGYIGSR)
- 多肽序列:H-Cys-Asp-Pro-Gly-Tyr-Ile-Gly-Ser-Arg-OH
- 单字母序列:H-CDPGYIGSR-OH
- 二硫键连接:无(序列仅含 1 个半胱氨酸残基,无法形成分子内二硫键;可通过该残基实现肽段的交联或载体偶联)
- 等电点(pI):理论值 8.0-8.5(含 1 个碱性氨基酸 Arg,1 个酸性氨基酸 Asp,整体呈弱碱性)
- 分子量:约 967.07Da
- 分子式:C40H62N12O14S
- 外观与溶解性:白色粉末,纯度≥98%;易溶于水、PBS 缓冲液(pH 7.0-7.5),微溶于甲醇、乙醇,不溶于氯仿、乙醚等非极性溶剂;水溶液浓度达 10 mg/mL 时无聚集、无浑浊,稳定性优异。
- 稳定性:-20℃干燥避光条件下可保存 24 个月以上;水溶液在 4℃下稳定 10 天,37℃生理条件下半衰期约 16 小时;序列中的 Pro 残基可增强肽链构象稳定性,抵抗部分蛋白酶水解。
- 结构式:
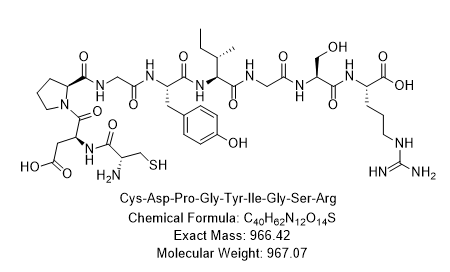
1. 核心生物活性
Laminin (925-933) 主要通过调控细胞与细胞外基质的粘附信号通路发挥功能,具体活性表现为:
- 强效细胞粘附与铺展:可促进内皮细胞、成纤维细胞、神经『干细胞』等多种细胞在基质表面的粘附与铺展,显著提升细胞存活率,效果优于单独的 YIGSR 五肽。
- 细胞迁移与分化调控:诱导细胞定向迁移,促进神经『干细胞』向神经元分化,加速皮肤创面的上皮化进程和血管新生。
- 组织修复与再生:在皮肤缺损、神经损伤、心肌缺血等模型中,可加速组织修复,提升再生组织的功能恢复水平。
- 『肿瘤』侵袭抑制:竞争性阻断『肿瘤』细胞表面整合素受体与层粘连蛋白的结合,抑制『肿瘤』细胞的侵袭、迁移及远处转移能力。
2. 作用机理
该肽段的生物活性基于受体介导的信号通路激活,具体机制如下:
- 受体特异性结合
- 肽段核心区 “YIGSR” 的 Tyr 残基芳香环嵌入整合素受体的疏水结合口袋,Arg 残基通过静电作用与受体的 Asp/Glu 残基结合,形成稳定的肽 - 受体复合物。
- N 端 “CDPG” 柔性区可增强肽链与受体的接触面积,提升结合亲和力。
2.下游信号通路激活
- FAK-Src 通路:受体活化后招募黏着斑激酶(FAK)和 Src 激酶,磷酸化下游信号分子,促进细胞骨架重组,调控细胞迁移与铺展。
- PI3K-Akt 通路:激活后抑制细胞凋亡相关蛋白(如 Caspase-3)的表达,提升细胞在应激环境下的存活率,加速组织修复。
- 『肿瘤』转移抑制机制:竞争性结合『肿瘤』细胞表面的整合素受体,阻断『肿瘤』细胞与细胞外基质的粘附,抑制基质金属蛋白酶(MMP-2/9)的分泌,降低『肿瘤』细胞的侵袭能力。
1. 主要应用领域
- 再生医学研究:用于皮肤创面愈合、神经损伤修复、心肌组织再生等模型的机制研究与候选药物开发。
- 『肿瘤』生物学研究:作为『肿瘤』转移机制研究的工具肽,探索整合素受体在『肿瘤』侵袭中的作用靶点。
- 生物材料表面修饰:通过 Cys 残基的巯基实现肽段与支架材料的共价偶联,构建具有细胞靶向性的组织工程支架。
- 靶向药物载体开发:偶联于纳米药物载体表面,实现药物向整合素高表达『肿瘤』组织或损伤组织的靶向递送。
2. 应用原理
- 再生医学应用原理:局部给药或材料表面修饰后,肽段靶向激活损伤部位细胞的整合素受体,促进细胞迁移、增殖与分化,加速受损组织的结构重建与功能恢复。
- 『肿瘤』研究原理:利用其与整合素受体的竞争性结合特性,阻断『肿瘤』细胞的粘附 - 侵袭通路,为『肿瘤』转移抑制剂的开发提供靶点和筛选工具。
- 生物材料修饰原理:通过巯基 - 马来酰亚胺反应将肽段固定于支架表面,为细胞提供特异性粘附位点,引导细胞定向生长,提升组织工程支架的生物相容性。
- 靶向药物载体原理:肽段偶联的纳米载体可通过受体介导的内吞作用,实现药物在病变组织的富集,降低药物对正常组织的毒副作用。
- 结构优化与活性提升:通过对序列进行环化修饰(利用 Cys 残基形成分子内二硫键),开发出的环肽衍生物半衰期延长至 48 小时,受体亲和力提升 3 倍,在小鼠皮肤创面模型中愈合效率提升 50%。
- 组织工程应用进展:将 CDPGYIGSR 修饰的聚己内酯(PCL)支架用于大鼠坐骨神经缺损修复,术后 12 周,再生神经的轴突数量和髓鞘厚度显著高于未修饰支架组,大鼠运动功能恢复评分提升 60%。
- 『肿瘤』靶向治疗研究:CDPGYIGSR 偶联的紫杉醇脂质体对整合素 α₆β₁高表达的肺癌细胞具有显著靶向杀伤效果,体内抑瘤率达 82%,且对小鼠正常组织的毒性显著低于游离紫杉醇。
- 『干细胞』分化调控研究:在神经『干细胞』培养体系中加入该肽段,可显著促进『干细胞』向胆碱能神经元分化,分化效率提升至 75%,为神经退行性疾病的细胞治疗提供了新策略。
- 皮肤创面愈合案例:在大鼠全层皮肤缺损模型中,局部应用含 CDPGYIGSR 的水凝胶敷料,与空白水凝胶组相比,创面愈合时间缩短 40%。组织学分析显示,处理组的新生血管密度增加 70%,胶原蛋白排列更规整,皮肤弹性恢复更优。
- 『肿瘤』转移抑制案例:在小鼠黑色素瘤肺转移模型中,腹腔注射 CDPGYIGSR 可使肺转移结节数量减少 65%。体外实验证实,该肽可抑制黑色素瘤细胞的侵袭能力,下调 MMP-9 的表达水平。
- 神经再生案例:将 CDPGYIGSR 修饰的壳聚糖导管用于大鼠脊髓半横断损伤修复,术后 8 周,损伤部位的神经轴突再生长度达 5 mm,显著长于未修饰导管组(2 mm),大鼠的运动功能评分提升 55%。



